- Gestion des processus d'entreprise (BPM)Système de gestion des documents (SGD)Système électronique de gestion de la qualité (QMS)Risque, gouvernance et conformité (GRC)Développement rapide d'applications à faible code (LC)Gestion de la continuité des activités (BCM)Architecture d'entreprise (EA)Gestion des processus d'entreprise (BPM)
- Vue d’ensemble de la gestion des processus d’entreprise
- Analyse, génération, amélioration et exploration des processus par l’intelligence artificielle
- Cartographie / modélisation des processus
- Analyse et amélioration des processus
- Simulation des processus
- Exploration de processus/process mining
- Collaboration et gouvernance
- Migration et intégration des données
- Application hors-ligne d’Interfacing
 Système de gestion des documents (SGD)
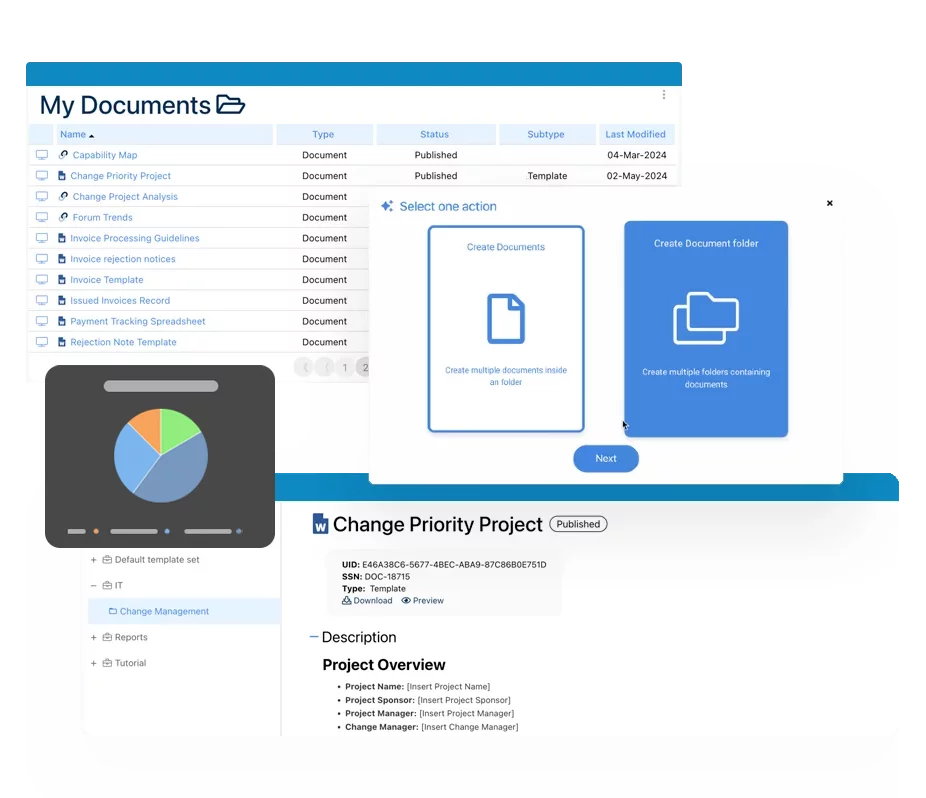
Système de gestion des documents (SGD)- Vue d’ensemble du contrôle des documents
- Création et amélioration du contenu avec l’intelligence artificielle
- Gestion des politiques et procédures (SOP)
- Parseur d’extraction de contenu de documents
- Collaboration et gouvernance
- Migration et intégration des données
- Application hors-ligne d’Interfacing
 Système électronique de gestion de la qualité (QMS)
Système électronique de gestion de la qualité (QMS)- Vue d’ensemble du système de gestion de la qualité
- Contrôle des documents et gestion des archives
- Gestion de l’audit et de l’accréditation
- Action corrective et préventive
- Événement de qualité (Non-conformité/plaintes/conformité)
- Gestion des risques
- Gestion des incidents
- Santé et sécurité environnementales
- Gestion des produits et des fournisseurs (SCAR)
- Gestion de la formation
- Gestion du contrôle
- Gestion des actions
- Examen de la gestion
- AMDE
- Pharmacovigilance
- Migration et intégration des données
 Risque, gouvernance et conformité (GRC)
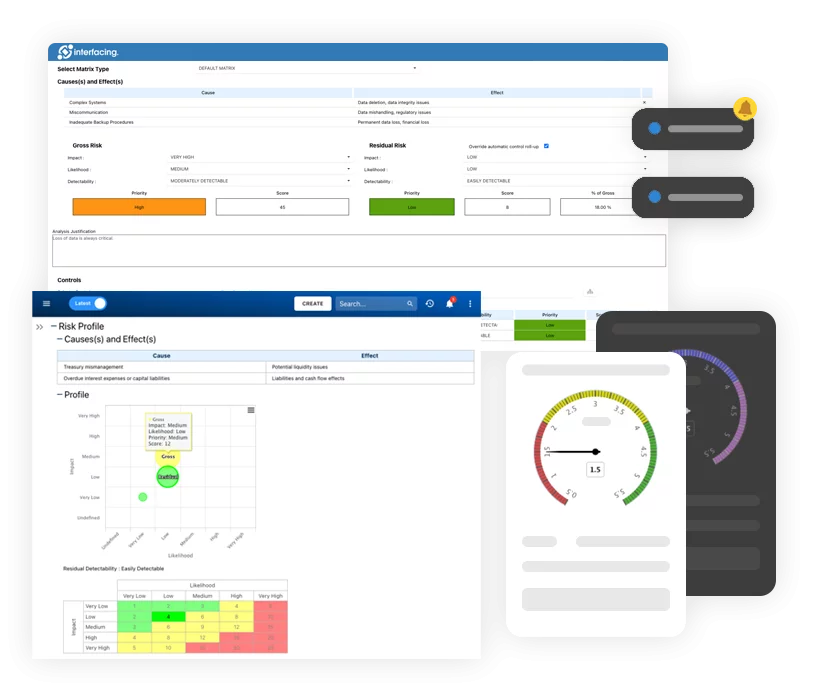
Risque, gouvernance et conformité (GRC)- Vue d’ensemble de la gestion des risques, de la gouvernance et de la conformité
- Gestion des risques et des contrôles
- Collaboration et gouvernance
- Migration et intégration des données
- Application hors-ligne d’Interfacing
 Développement rapide d'applications à faible code (LC)
Développement rapide d'applications à faible code (LC)- Vue d’ensemble de la plateforme d’automatisation à faible code
- Conception de formulaires électroniques (eFORMS)
- Concepteur d’entité de table de base de données
- Concepteur de l’intégration des systèmes
- Conception et gestion des tâches
- Règles, gardes et actions personnalisées
- Services de messagerie textuelle et vocale
- BAM (Business Activity Monitoring)
- Conception d’un tableau de bord personnalisé
- Migration et intégration de données
 Gestion de la continuité des activités (BCM)
Gestion de la continuité des activités (BCM)- Vue d’ensemble de la gestion de la continuité des activités
- Analyse d’impact sur les affaires
- Simulation de reprise après sinistre
- Gestion des actions
- Gestion des notifications de masse
- Gestion des actifs
- Migration et intégration des données
 Architecture d'entreprise (EA)
Architecture d'entreprise (EA) - Les industriesConformité réglementaireCas d'utilisationCentre d'apprentissageCadre et pratiquesLes industries
- Santé
- Technologies médicales
- Pharmaceutique
- Aérospace et Défense
- Aériennes et Aviation
- Médias et Télécommunications
- Gouvernemental et Militaire
- Technologie
- Énergie
- Opérations logistiques et portuaires
- Banque et marchés de capitaux
- Commerce de détail et consommation
- Services de Consultation
- Éducation
- Ingénierie et construction
- Fabrication
- Services Financiers
- Assurance
- Produits Chimiques
Conformité réglementaireCas d'utilisationCentre d'apprentissageCadre et pratiques - À propos de nousSuccès clientProgramme de partenariatÀ propos de nousSuccès clientProgramme de partenariat



Conformité ISO 13485 pour les dispositifs médicaux
Please Select contact form.
Garantissez la qualité, la sécurité et la conformité réglementaire de la fabrication de dispositifs médicaux grâce aux outils de conformité propulsés par l’IA d’Interfacing.

Qu'est-ce que l’ISO 13485 ?
La conformité à la norme ISO 13485 fait référence au respect de la norme internationale ISO 13485, qui précise les exigences relatives à un système de gestion de la qualité (SGQ) spécifiquement conçu pour l’industrie des dispositifs médicaux. Introduite en 1996 et révisée pour la dernière fois en 2016, l’ISO 13485 est basée sur la norme ISO 9001, mais intègre des exigences réglementaires supplémentaires propres au secteur de la santé.
La norme vise à garantir que les dispositifs médicaux et les services connexes répondent de manière constante aux attentes des clients et aux exigences réglementaires. Contrairement à l’ISO 9001, l’ISO 13485 met l’accent sur la gestion des risques, le contrôle de la conception, des procédures de documentation rigoureuses et le maintien de processus efficaces tout au long du cycle de vie du produit — y compris la surveillance post-commercialisation.
Comment l’IA transforme la conformité à l’ISO 13485
La gestion manuelle de la conformité est lente, sujette aux erreurs et coûteuse. L’intelligence artificielle (IA) aide les organisations non seulement à respecter les exigences, mais aussi à anticiper les changements.
Voici comment l’IA accélère la conformité à l’ISO 13485 :
- L’exploration de processus assistée par IA détecte les goulets d’étranglement dans les flux de travail SGQ.
- Le traitement du langage naturel extrait des informations à partir de rapports d’audit, de dossiers de non-conformité et de documents fournisseurs.
- L’analyse prédictive signale les écarts à haut risque et prévient les problèmes réglementaires.
- Des formulaires intelligents et des flux de travail dynamiques simplifient le contrôle documentaire, les enregistrements de formation et l’approbation des procédures.
En intégrant l’IA dans leur cadre de conformité, les entreprises améliorent leur préparation aux audits, réduisent les erreurs manuelles et restent alignées sur les règlements en constante évolution.


Pourquoi la conformité ISO 13485 est-elle importante ?
Les réglementations mondiales sur les dispositifs médicaux sont de plus en plus harmonisées, et l’ISO 13485 est devenue la norme de référence pour démontrer la conformité. Par exemple :
- En Europe, l’ISO 13485 est alignée avec le Règlement sur les dispositifs médicaux (MDR) et le Règlement sur les dispositifs de diagnostic in vitro (IVDR).
- Dans les secteurs de la santé et de la pharmaceutique, où la sécurité des patients et la qualité des données sont essentielles.
- Au Canada, la certification ISO 13485 est requise pour obtenir la licence des dispositifs médicaux de classe II, III et IV.
En résumé : la certification ISO 13485 ne se limite pas à cocher des cases — elle constitue une autorisation d’opérer sur les marchés internationaux. Surtout, c’est un cadre proactif pour réduire les rappels de produits, atténuer les risques pour les patients et améliorer les résultats cliniques.


Qui doit se conformer à l’ISO 13485 ?
La norme ISO 13485 s’applique à un large éventail d’organisations dans la chaîne d’approvisionnement des dispositifs médicaux :
- Fabricants d’équipements d’origine (OEM)
- Fournisseurs de composants et de matériaux
- Services de stérilisation et d’emballage sous contrat
- Développeurs de logiciels utilisés comme dispositifs médicaux (SaMD)
- Consultants réglementaires et représentants autorisés

Cas d’utilisation dans le monde réel : ISO 13485 en action
Entreprise : MedTech Innovators Inc.
Défi : Cette entreprise canadienne de taille moyenne développe des dispositifs cardiovasculaires de classe III. Elle devait accéder au marché européen, mais ne disposait pas d’une documentation et d’une traçabilité structurées pour ses processus de recherche et de développement.
La solution : En adoptant la norme ISO 13485 avec l’aide de la Digital Business Platform de Interfacing, l’entreprise.. :
- Réalisation d’une analyse complète des écarts par rapport aux clauses de la norme ISO 13485
- Utilisation de la modélisation des processus pour cartographier les étapes du développement des produits
- IA intégrée pour signaler automatiquement les non-conformités et les révisions de documents
- Réussir l’audit d’une tierce partie dans un délai de neuf mois
- Obtention du marquage CE et développement des ventes dans l’UE
L’impact : Après la certification, MedTech Innovators a réduit de 60 % le temps de préparation des audits et son taux d’incidents de qualité a chuté de 35 % au cours de la première année.
Principales exigences de la norme ISO 13485
Les principaux domaines couverts par la norme sont les suivants :
- Contrôle des documents : Maintenez des procédures et des dossiers cohérents et à jour.
- Gestion des risques : Abordez les risques tout au long du cycle de vie du produit, de la conception au déclassement.
- Validation : Veillez à ce que tous les processus (en particulier les logiciels et la stérilisation) soient validés et traçables.
- Qualité des fournisseurs : Évaluer et contrôler les fournisseurs en fonction des critères de conformité.
- Actions correctives et préventives (CAPA) : Suivez les non-conformités et mettez en œuvre des améliorations fondées sur des données.
- Surveillance après la mise sur le marché : Recueillir et analyser les données de terrain afin d’améliorer les produits.
Steps to ISO 13485 Certification
Étapes vers la certification ISO 13485
La certification ISO 13485 comprend plusieurs étapes structurées visant à aligner votre organisation avec les attentes réglementaires et les meilleures pratiques de gestion qualité :
-
Réaliser une analyse des écarts
Évaluer vos processus, documents et systèmes actuels par rapport aux exigences de l’ISO 13485. Identifier les lacunes et faiblesses. La plateforme Interfacing offre des outils d’analyse alimentés par l’IA pour accélérer cette étape. -
Définir la portée et les objectifs
Déterminer les limites du SGQ (produits, sites, départements) et établir des objectifs qualité alignés sur les exigences réglementaires et les buts stratégiques. -
Cartographier et documenter les processus
Documenter les processus, politiques et procédures qualité de façon claire, cohérente et traçable. Utilisez les outils de modélisation d’Interfacing pour garantir l’alignement avec les clauses de l’ISO. -
Mettre en œuvre les contrôles et attribuer les rôles
Mettre en place des contrôles pour la gestion du changement, des risques, des fournisseurs, de la formation, et des CAPA. Définir clairement les responsabilités. -
Former les équipes et déployer le système
Former le personnel sur les nouvelles procédures. S’assurer que le SGQ est effectivement appliqué au quotidien. Interfacing facilite les suivis de formation, la gestion des SOP et la vérification des compétences. -
Effectuer des audits internes et appliquer les CAPA
Réaliser des audits internes pour vérifier la performance du SGQ et corriger les non-conformités. Interfacing automatise les pistes d’audit et relie les tâches CAPA aux processus. -
Effectuer une revue de direction
Les dirigeants doivent évaluer l’efficacité du SGQ à partir des résultats d’audit, des retours clients, des indicateurs de risque et de l’efficacité des CAPA. Les tableaux de bord Interfacing facilitent cette revue. -
Choisir un organisme de certification accrédité
Faire appel à un certificateur reconnu (ex. : BSI, TÜV SÜD, SGS). L’audit se déroule en deux étapes : revue documentaire (Étape 1) et audit complet sur le terrain (Étape 2). -
Obtenir la certification
Une fois l’audit réussi, votre organisation reçoit le certificat ISO 13485 (valide pour 3 ans, avec audits de surveillance annuels). -
Maintenir et améliorer continuellement
L’ISO 13485 est un engagement à long terme. Utilisez l’IA et les analyses de processus pour surveiller la performance, adapter vos pratiques, et rester toujours prêt pour les audits.
Comment Interfacing contribue à la mise en œuvre de la norme ISO 13485
InterfacingLa plateforme d’entreprise numérique d’EMC est spécialement conçue pour soutenir la conformité à la norme ISO 13485 des entreprises de dispositifs médicaux. Nos outils permettent d’unifier les fonctions de qualité, de risque et de réglementation dans l’ensemble de l’entreprise.
Ce que nous offrons :
Outils d’analyse des écarts directement liés aux clauses de la norme ISO 13485
Modélisation visuelle des processus et contrôle du cycle de vie des documents
Pistes d’audit automatisées, versions et signatures électroniques
Des actions correctives et des optimisations de processus suggérées par l’IA
Tableaux de bord intégrés pour un suivi de la conformité en temps réel
Avec Interfacing, votre système de conformité ne se contente pas de cocher une case, il devient un avantage stratégique.

Ensure Process & Quality Governance
Interfacing’s Enterprise Process Center® (EPC) allows you to define, document, and enforce ISO 9001 quality controls organization-wide. Policies, procedures, and SOPs are directly tied to processes and roles—ensuring your QMS is embedded in everyday operations with full transparency. .

Eliminate Manual Errors with AI-Driven QMS
Standardizing documentation and workflows within EPC removes the need for spreadsheets and disconnected systems. Our AI flags outdated procedures, suggests process improvements, and helps maintain version control—reducing the risk of non-compliance and audit issues.

Gain Full Audit Readiness & Traceability
EPC provides real-time traceability across all quality processes—from document approvals to CAPA workflows. With automated audit trails and visual process maps, you’re always ready for certification audits and internal reviews, no last-minute scrambling required

Improve Operational Efficiency Without Sacrificing Compliance
Interfacing’s QMS automates routine tasks such as change control, training sign-offs, and document updates. This not only frees up valuable staff time, but also ensures consistent adherence to ISO 9001 guidelines across all departments and geographies.

Reduce the Cost of Quality Compliance
With centralized process governance and AI-enhanced workflows, EPC reduces the overhead of maintaining your QMS. From smarter audit prep to fewer non-conformities, organizations save time, cut errors, and accelerate their path to ISO 9001 certification.

Build a Culture of Continuous Improvement
ISO 9001 is about more than passing audits—it’s about evolving your organization. Interfacing’s platform helps identify quality gaps, track corrective actions, and promote ongoing learning and accountability—turning compliance into a competitive advantage.
Pourquoi choisir Interfacing?
Avec plus de deux décennies de logiciels d'IA, de qualité, de processus et de conformité, Interfacing continue d'être un leader dans l'industrie. À ce jour, nous avons servi plus de 500+ entreprises de classe mondiale et des sociétés de conseil en gestion de toutes les industries et de tous les secteurs. Nous continuons à fournir des solutions numériques, cloud et IA qui permettent aux organisations d'améliorer, de contrôler et de moderniser leurs processus tout en allégeant le fardeau de la conformité réglementaire et des programmes de gestion de la qualité.
Pour en savoir plus ou discuter de la manière dont Interfacing peut aider votre organisation, veuillez remplir le formulaire ci-dessous.

Documentation : Piloter la transformation, la gouvernance et le contrôle
• Obtenez des informations complètes et en temps réel sur vos opérations.
• Améliorez la gouvernance, l'efficacité et la conformité.
• Assurez une conformité fluide avec les normes réglementaires.

eQMS : Automatiser les workflows de qualité et de conformité & rapports
• Simplifiez la gestion de la qualité avec des workflows automatisés et une traçabilité continue.
• Standardisez la gestion des CAPA, des audits fournisseurs, de la formation et des workflows associés.
• Transformez la documentation en informations exploitables pour la Qualité 4.0.

Développement rapide d'applications low-code : Accélérer la transformation numérique
• Créez rapidement des applications personnalisées et évolutives.
• Réduisez le temps et les coûts de développement.
• Adaptez-vous rapidement pour répondre aux besoins évolutifs des clients et de votre entreprise.
L’IA pour transformer votre entreprise !
Conçus pour optimiser les opérations, l'efficacité et renforcer la conformité. Découvrez nos solutions alimentés par l’IA :
• Répondre aux questions des employés.
• Transformer des vidéos en processus.
• Recommander des améliorations de processus et des impacts réglementaires.
• Générer des formulaire, processus, risques, réglementations, KPIs, et bien plus.
• Fragmenter les normes réglementaires

Demandez une démo gratuite
Documentez, analysez, améliorez, numérisez et surveillez vos processus, vos risques, vos exigences réglementaires et vos indicateurs de performance au sein du système de gestion intégré Digital Twin d’Interfacing, l’Enterprise Process Center®!
Approuvé par nos clients à travers le monde !
Plus de 400 entreprises de classe mondiale et cabinets de conseil en gestion.



















































INTEGRATION
Approuvé par les nos clients dans le monde entier !
Plus de 400 entreprises de classe mondiale et cabinets de conseil en gestion.




























