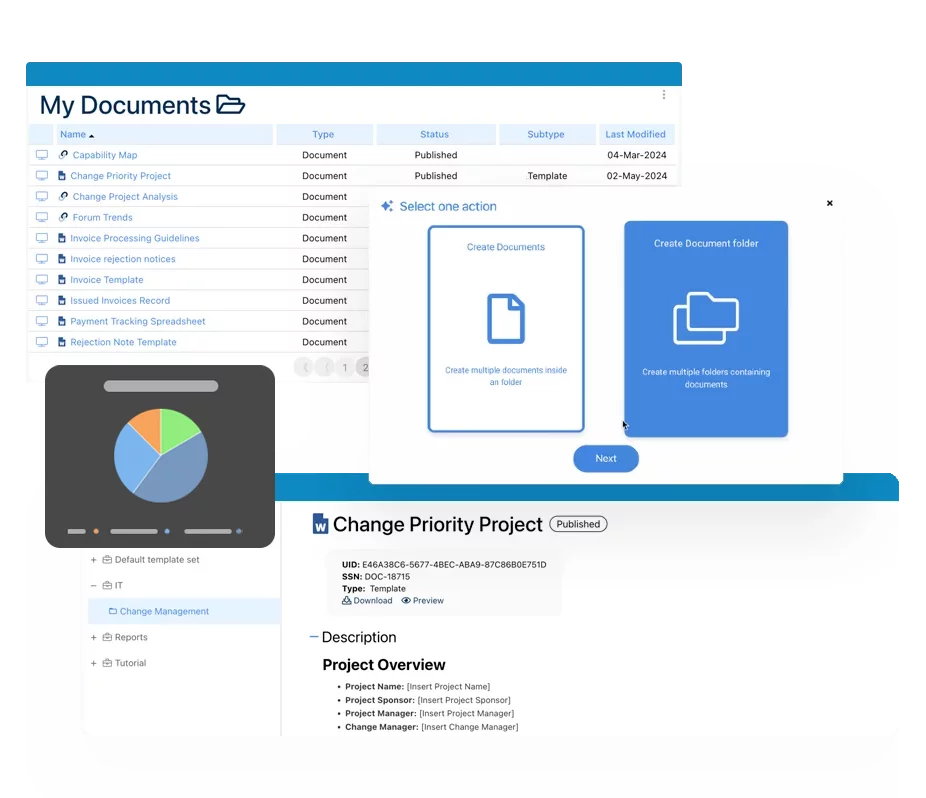
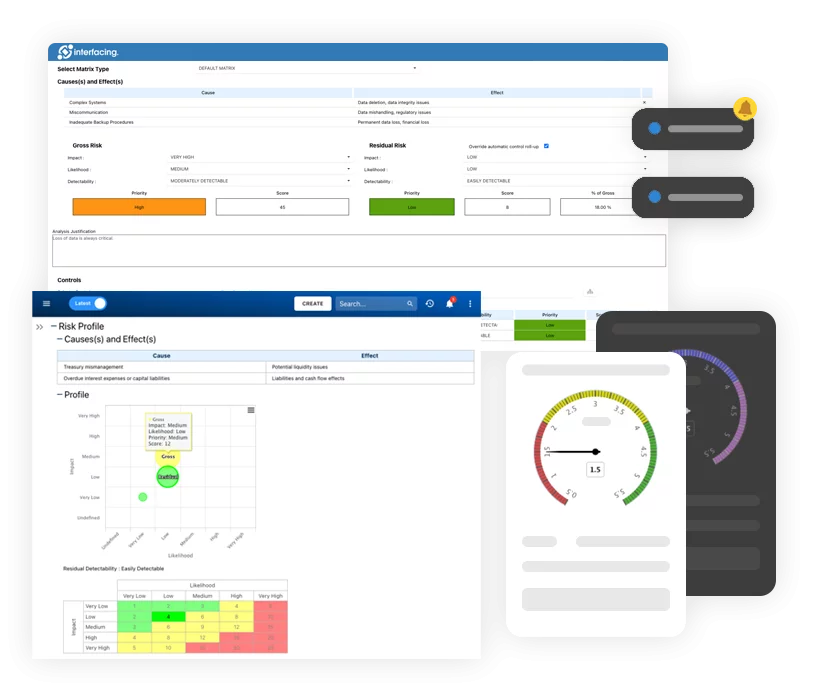
BPM comme moteur de la transformation numérique des QMS dans les industries réglementées GxP
Please Select contact form.
Favoriser la conformité, l'efficacité et l'innovation grâce à l'automatisation des processus

Résumé
Bien que la gestion des processus métier (BPM) se soit révélée extrêmement utile pour divers cas d'utilisation dans de nombreuses industries et fonctions au fil des décennies, elle reste encore largement sous-utilisée dans les processus essentiels des industries réglementées GxP. Cet article résume les éléments traditionnels des systèmes de gestion de la qualité (QMS). La conclusion est que ces systèmes ne sont pas numérisables dans leur cadre actuel. En revanche, les méthodes et outils du BPM peuvent être utilisés pour développer des parcours de transformation.
Introduction
Dans une définition simple, une « industrie réglementée » est étroitement surveillée par des organismes gouvernementaux. Dans ce sens, de nombreuses industries (voire toutes) sont « réglementées ». Des exemples évidents sont les services financiers, l'aviation et l'industrie pharmaceutique. Du point de vue de l'entreprise, la réglementation est étroitement liée à ce que l'on appelle la « licence d'exploitation » : « aucune conformité » signifie aucune autorisation de fournir des services ou de produire des biens.
Le terme GxP regroupe toutes les lignes directrices pour les « bonnes pratiques de travail ». Le « G » signifie « Good » (bon), le « P » pour « Practice » (pratique), et le « x » au milieu est remplacé par l'abréviation respective du domaine d'application spécifique.
Des lignes directrices similaires pour le secteur pharmaceutique ont été préparées, par exemple, par l'Agence européenne des médicaments (EMA), la Food and Drug Administration (FDA) des États-Unis et, à l'échelle mondiale, par le Conseil international pour l'harmonisation des exigences techniques relatives aux produits pharmaceutiques à usage humain (ICH).
Les Bonnes pratiques de fabrication (Good Manufacturing Practice - GMP) constituent une ligne directrice pour l'assurance qualité dans la production de produits pharmaceutiques. Des lignes directrices similaires s'appliquent à la fabrication de dispositifs médicaux, de cosmétiques et d'aliments. Les principes de base d'un système de gestion de la qualité (QMS) sont généralement mis en œuvre dans l'industrie chimique, même si celle-ci n'est pas réglementée par GxP.
Méthodes et outils du BPM : une histoire de succès
La gestion des processus a contribué à des améliorations substantielles au cours des deux dernières décennies grâce à ses méthodes et outils dans de nombreux domaines.
À titre d’exemples : Projets d’introduction du logiciel SAP, Systèmes de gestion basés sur la norme ISO 9001, Gestion des risques

Succès limité dans l'industrie réglementée GxP
Contrairement aux succès mentionnés ci-dessus, le BPM dans l'industrie réglementée GxP reste limité. Il est vrai que, par exemple, dans les projets informatiques (notamment dans le contexte de SAP) ou dans les initiatives d'Excellence Opérationnelle, des contributions significatives au succès de l'entreprise ont été apportées. Un domaine en pleine expansion consiste à contrôler les services internes via des processus, à condition qu'ils ne soient pas liés à la réglementation GxP. Néanmoins, on peut dire que la gestion des processus ne joue pas un rôle majeur dans les processus essentiels.

Éléments d'un système de gestion de la qualité conforme aux GxP
Pour comprendre la situation initiale, il est nécessaire de noter ce qui constitue un QMS conforme aux GxP :
- Gestion des réglementations
- Qualification / Validation
- Gestion des écarts
- Gestion des changements
- Formation des employés
- Gestion des risques
- Audits internes
Comme les points 2 à 7 ci-dessus sont basés sur la gestion des réglementations, il devient évident qu'un QMS basé sur les GxP est orienté par des réglementations et donc par des documents historiquement établis. Bien sûr, différents types de documents doivent être distingués, par exemple les procédures opératoires standardisées (SOP), les instructions opérationnelles et les formations.
Même si les SOP ne sont pas structurées (c’est-à-dire en « texte libre »), des éléments individuels peuvent être identifiés et appliqués aux processus :
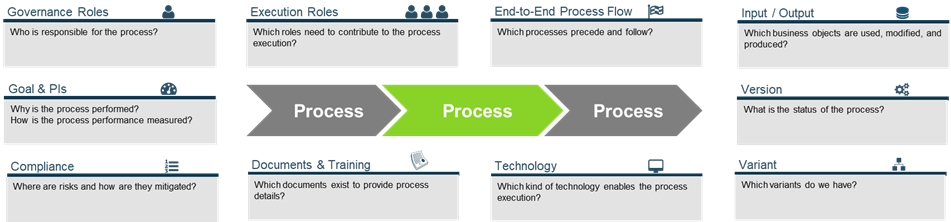
- Rôles de gouvernance
- Rôles d’exécution
- Activités (tâches, événements, passerelles)
- Termes et définitions
- Références aux réglementations externes
En d'autres termes, une procédure décrit un processus. Mais si tous les processus essentiels sont déjà décrits sous forme de documents, que peut faire la gestion des processus pour les améliorer ?

L'état actuel et ses inconvénients
Les documents ont déjà connu une longue histoire de transformation.
Bien qu’ils présentent des avantages (un système complet qui fonctionne pour l’objectif prévu, c’est-à-dire qu’il est conforme), des faiblesses et des limites deviennent de plus en plus apparentes au quotidien : des efforts considérables sont enregistrés comme « coût de conformité ». Cela comprend :
- Efforts de création des documents
- Efforts de modification des documents – le changement en masse n’est pas possible en raison des données non structurées
- Redondances et contradictions entre les documents, par exemple, des rôles et des termes définis à plusieurs endroits et de manière différente
- Temps nécessaire pour trouver des informations pertinentes dans les documents
En plus de ces désavantages quantitatifs, les employés se plaignent également de deux aspects qualitatifs qui semblent contradictoires : d’une part, les documents sont beaucoup trop généraux (je reçois beaucoup d'informations qui ne me concernent pas ou qui ne concernent pas mon rôle). D'autre part, la « vue d'ensemble » manque. L’accent est mis sur le document individuel, tandis que l’objectif, le processus de bout en bout ou le bénéfice client ne sont pas visibles.
Dans l’ensemble, le QMS est un paysage constitué de réglementations locales indépendantes, avec de nombreuses redondances et des coûts globaux élevés.
Objectifs et opportunités de la numérisation
Tout d’abord, il faut tenir compte du fait que des milliers de documents, voire des centaines de milliers dans les très grandes entreprises et sur tous les sites, sont concernés. D’autre part, la pression temporelle est limitée si nous supposons qu’il existe un système de gestion de la qualité opérationnel.
L’objectif est de mettre en place une solution entièrement numérique. Dans la pratique, les avantages suivants ont été démontrés :
- Le principe de réutilisation des données de base (établi dans les processus financiers et de marchandises, par exemple dans SAP depuis les années 1990) contribue à réduire la duplication du travail.
- Modifications de masse simples : étant donné que les informations utilisées sont claires, il est possible de procéder à des modifications de masse.
- L’ expérience de l’utilisateur doit être conforme aux normes actuelles, voire les dépasser (voir ISO 13407 “Conception orientée vers l’utilisateur des systèmes interactifs”). Il en résulte une plus grande efficacité et une meilleure acceptation de la part des destinataires de l’information.
- Une conception essentiellement graphique repose sur l’idée que le traitement de l’information visuelle chez l’homme est incroyablement efficace et qu’il est possible de faire tenir beaucoup d’informations dans un espace réduit.
- Capacités mobiles et multimédias : tout avoir sur son ordinateur de poche est une nécessité, tandis que l’intégration de vidéos sur les activités correspondrait à votre niveau de maturité le plus élevé.
- Personnalisation : Les utilisateurs voient le contexte global mais peuvent filtrer très précisément si nécessaire, par exemple en fonction de leur rôle d’exécution : qu’est-ce qui est pertinent pour moi ?
Les étapes d’une transformation
- Une carte des processus garantit que, d’une part, tous les sujets sont enregistrés (exhaustivité) et que, d’autre part, il n’y a pas de chevauchements. En comparant les procédures existantes, vous constaterez rapidement que la transformation part d’un état “many to many”. Cela signifie que le contenu pertinent pour un processus se trouve dans plusieurs procédures. Inversement, cependant, une procédure contient généralement aussi des informations pour plusieurs processus.
- En outre, comme indiqué ci-dessus, il existe des informations “globales” à caractère master data , par exemple les rôles de gouvernance, les rôles d’exécution, les termes. Ces informations ne sont créées qu’une seule fois dans une solution numérique et peuvent être référencées à partir de là.
- Sélectionnez une plateforme informatique de niveau supérieur: il existe aujourd’hui sur le marché des outils innovants qui gèrent tous les processus et le contenu des POS en tant qu’informations tout en appliquant les exigences de conformité pharmaceutique telles que la gestion des changements, l’évaluation de l’impact, l’approbation et les flux de travail de gouvernance, y compris les signatures numériques conformes à la norme FDA 21 CFR part 11.
Transformation numérique du système de gestion de la qualité : exemple de feuille de route

Pourquoi choisir Interfacing?
Avec plus de deux décennies de logiciels d'IA, de qualité, de processus et de conformité, Interfacing continue d'être un leader dans l'industrie. À ce jour, nous avons servi plus de 500+ entreprises de classe mondiale et des sociétés de conseil en gestion de toutes les industries et de tous les secteurs. Nous continuons à fournir des solutions numériques, cloud et IA qui permettent aux organisations d'améliorer, de contrôler et de moderniser leurs processus tout en allégeant le fardeau de la conformité réglementaire et des programmes de gestion de la qualité.
Pour en savoir plus ou discuter de la manière dont Interfacing peut aider votre organisation, veuillez remplir le formulaire ci-dessous.

Documentation : Piloter la transformation, la gouvernance et le contrôle
• Obtenez des informations complètes et en temps réel sur vos opérations.
• Améliorez la gouvernance, l'efficacité et la conformité.
• Assurez une conformité fluide avec les normes réglementaires.

eQMS : Automatiser les workflows de qualité et de conformité & rapports
• Simplifiez la gestion de la qualité avec des workflows automatisés et une traçabilité continue.
• Standardisez la gestion des CAPA, des audits fournisseurs, de la formation et des workflows associés.
• Transformez la documentation en informations exploitables pour la Qualité 4.0.

Développement rapide d'applications low-code : Accélérer la transformation numérique
• Créez rapidement des applications personnalisées et évolutives.
• Réduisez le temps et les coûts de développement.
• Adaptez-vous rapidement pour répondre aux besoins évolutifs des clients et de votre entreprise.
L’IA pour transformer votre entreprise !
Conçus pour optimiser les opérations, l'efficacité et renforcer la conformité. Découvrez nos solutions alimentés par l’IA :
• Répondre aux questions des employés.
• Transformer des vidéos en processus.
• Recommander des améliorations de processus et des impacts réglementaires.
• Générer des formulaire, processus, risques, réglementations, KPIs, et bien plus.
• Fragmenter les normes réglementaires

Demandez une démo gratuite
Documentez, analysez, améliorez, numérisez et surveillez vos processus, vos risques, vos exigences réglementaires et vos indicateurs de performance au sein du système de gestion intégré Digital Twin d’Interfacing, l’Enterprise Process Center®!
Approuvé par nos clients à travers le monde !
Plus de 400 entreprises de classe mondiale et cabinets de conseil en gestion.



















































INTEGRATION
Approuvé par les nos clients dans le monde entier !
Plus de 400 entreprises de classe mondiale et cabinets de conseil en gestion.